Distúrbios de Coagulação
Definição: A ocorrência de coagulopatias é comum no ambiente de terapia intensiva. Seja como consequência de uma doença de base, seja como motivo da internação, os distúrbios da coagulação influenciam o prognóstico do paciente em estado crítico, aumentando sua morbi/mortalidade.
-
Padrão do sangramento:
- Mucocutâneo: Alteração da hemostasia primária (plaquetas ou fator de von Willebrand);
-
Hematomas de partes moles e hemartroses:
Alteração da hemostasia secundária (fatores de coagulação).
-
Tempo para o início do sangramento:
- Imediato: A lteração da hemostasia primária (plaquetas ou fator de von Willebrand);
-
Tardio:
A
lteração da hemostasia secundária (fatores de coagulação).
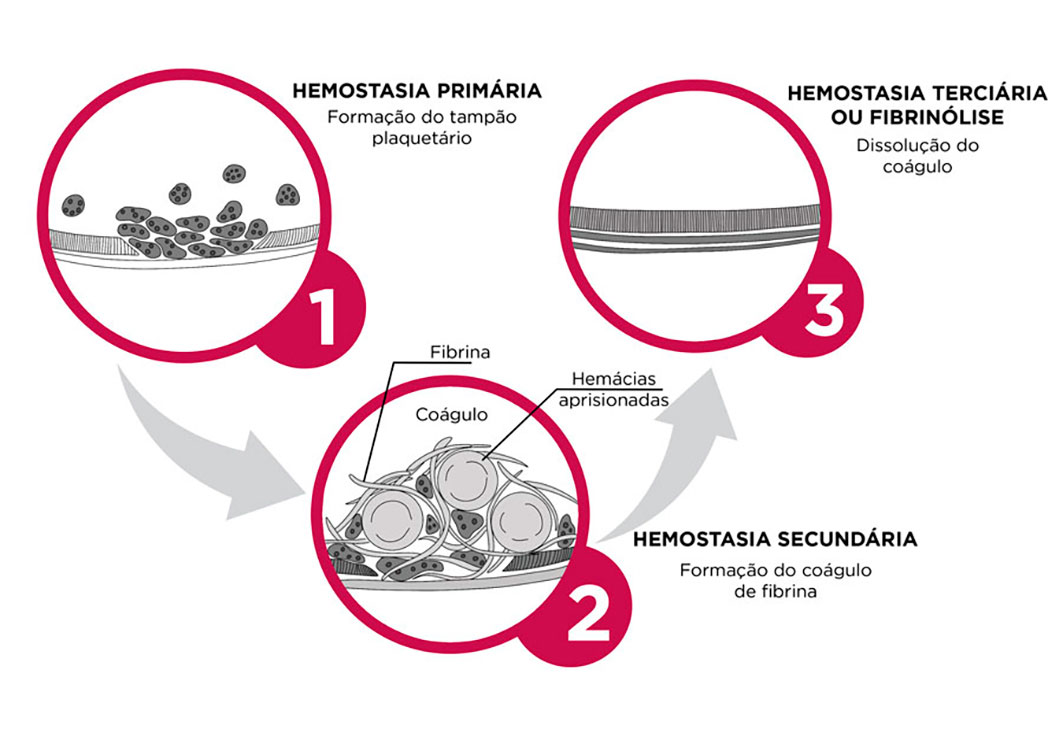 Etapas da hemostasia.
Ilustração:
Leandro Zamonel Rocha.
Etapas da hemostasia.
Ilustração:
Leandro Zamonel Rocha.
-
Exames laboratoriais iniciais:
- Contagem de plaquetas;
- Tempo de protrombina (TAP);
- Tempo de tromboplastina parcial ativada (PTTa);
- Tempo de trombina (TT) e fibrinogênio .
-
Diagnóstico diferencial conforme os testes de coagulação:
- PTTa prolongado e TAP normal, com TT normal: Uso de heparina não fracionada; deficiência ou inibidor de fatores VIII (hemofilia A ), IX (hemofilia B) ou XI (hemofilia C); doença de von Willebrand , detecção de anticoagulante lúpico;
-
PTTa normal e TAP prolongado, com TT normal:
Deficiência de vitamina K
ou uso de antagonista de vitamina K (Varfarina); hepatopatia; deficiência ou inibidor de fator VII
(condições raras);
-
PTTa e TAP prolongados, com TT normal:
Hepatopatia; intoxicação por Varfarina e Heparina; deficiência ou inibidor de protrombina (fator II) ou dos fatores V
ou X
(condições raras);
-
PTTa normal ou prolongado, TAP normal ou prolongado e TT prolongado:
Deficiência de fibrinogênio (qualitativa ou quantitativa), coagulação intravascular disseminada (CIVD).
Observação!
CIVD
pode prolongar PTTa, TAP e TT devido ao consumo de fatores de coagulação e fibrinogênio.
Trombocitopenia
Definição:
Plaquetas < 150.000/mm³.
A trombocitopenia
é comum em pacientes em estado crítico. A maior parte dos casos está relacionada com infecções, quimioterapia, toxicidade de medicamento(s) e CIVD. Está diretamente associada a um pior prognóstico, além de ser considerada um marcador de tempo de internação.
A maioria dos pacientes só apresenta sintomas quando os níveis de plaquetas estão abaixo de 50.000/mm³. O risco de sangramento espontâneo aumenta muito quando plaquetometria abaixo de 20.000/mm³.
-
Principais sinais e sintomas:
- Petéquias e equimoses;
-
Gengivorragia e epistaxe;
- Menorragia;
- Hemorragia intracraniana (rara, mas potencialmente fatal).
-
Principais situações:
- Indução por medicamentos (ex.: Furosemida, Ácido valproico, Ácido acetilsalicílico, betalactâmicos, Carbamazepina, Quinidina, Fenitoína, diurético tiazídico, Sulfametoxazol-Trimetoprima, Vancomicina) ou toxinas;
-
Microangiopatias trombóticas
(síndrome hemolítico-urêmica
, púrpura trombocitopênica trombótica
)
;
- CIVD;
-
Doenças autoimunes (ex.: lúpus eritematoso sistêmico
, síndrome do anticorpo antifosfolipídio
);
-
Hipertensão portal com hiperesplenismo;
-
Infecções bacterianas e virais (ex.: dengue
);
-
Destruição mecânica (ex.: valvopatias, dispositivos intravasculares como balão intra-aórtico);
- Destruição pós-transfusional ou transfusão maciça ;
- Gestação: Síndrome HELLP ou trombocitopenia gestacional .
-
Emergências médicas:
- Hemorragia na presença de trombocitopenia grave;
-
Necessidade urgente de procedimentos invasivos
na presença de trombocitopenia grave;
-
CIVD:
Desordem sistêmica caracterizada por ativação descontrolada do processo de coagulação sanguínea, com risco de trombose e hemorragia;
-
Trombocitopenia induzida por Heparina
(HIT, do inglês
H
eparin-Induced Thrombocytopenia
)
:
Pode ocorrer a
pós exposição à Heparina (não fracionada ou de baixo peso molecular), com formação de anticorpo anti-PF4, que ativa plaquetas causando fenômenos trombóticos arteriais e venosos;
-
Microangiopatia trombótica:
Caracteriza-se por trombocitopenia, anemia hemolítica
microangiopática e dano orgânico;
-
Trombocitopenia grave na gestação:
Deve-se avaliar possibilidade de síndrome HELLP, condição potencialmente fatal, caracterizada por hemólise, elevação das enzimas hepáticas e trombocitopenia.
-
Abordagem diagnóstica:
- Pseudotrombocitopenia (erro laboratorial): Primeira possibilidade a ser excluída. Deve-se avaliar a presença de agregados plaquetários, macroplaquetas e/ou satelitismo plaquetário na lâmina de sangue periférico e repetir a contagem em tubo com citrato (tampa azul – tubo de coagulograma);
- Recomenda-se a realização de exames complementares conforme a suspeita clínica (ex.: função hepática, coagulograma, pesquisa de autoanticorpos).
Atenção!
Púrpura trombocitopênica imune
é um diagnóstico de exclusão e predominantemente clínico.
-
Abordagem terapêutica:
- O manejo depende da causa de base;
- Em alguns casos, pode ser necessário submeter o paciente à transfusão de plaquetas : A indicação de transfusão deve ser avaliada individualmente (gravidade da trombocitopenia, sintomatologia, necessidade de procedimentos invasivos), sendo raramente realizada no contexto de destruição periférica de plaquetas;
-
Em geral, considera-se a transfusão quando:
Plaquetometria < 10.000/mm³; plaquetometria < 20.000/mm³ + fatores associados, como febre, eventos hemorrágicos, doença enxerto
versus
hospedeiro, queda rápida da plaquetometria, outras alterações da hemostasia; plaquetometria < 50.000/mm³ + proposta de procedimentos invasivos, exceto neurocirúrgicos e oftalmológicos; plaquetometria < 80.000-100.000/mm³ + proposta de procedimentos neurocirúrgicos ou oftalmológicos; associação com CIVD; hemorragia associada a defeito plaquetário qualitativo e refratária a outras medidas.
Para mais informações sobre trombocitopenia, acesse: Abordagem ao paciente com trombocitopenia.
Coagulação Intravascular Disseminada (CIVD)
Fenômeno decorrente do desequilíbrio entre fibrinólise e coagulação. Manifesta-se por súbita queda da quantidade de plaquetas, alargamento de todos os tempos de coagulação e consumo de fibrinogênio, associado ao aumento dos produtos de degradação da fibrina (D-dímero
). O paciente pode evoluir com sangramentos e/ou eventos tromboembólicos.
-
Principais causas no Centro de Tratamento Intensivo:
- Sepse – a mais frequente;
-
Neoplasias (ex.: leucemia promielocítica aguda
);
-
Insuficiência hepática
e pancreatite;
-
Distúrbios vasculares e imunológicos (ex.: reação transfusional hemolítica aguda
);
-
Intoxicações (ex.: veneno de cobra);
-
Trauma (ex.: lesão por esmagamento);
- Grande queimado;
-
Uso de substâncias (ex.:
overdose
de anfetamina);
-
Complicações obstétricas (ex.: pré-eclâmpsia
, abortamento retido
, síndrome HELLP
).
-
Abordagem diagnóstica:
-
O diagnóstico é clínico e laboratorial;
- Achados que sugerem o diagnóstico incluem: Trombocitopenia moderada a grave, história de trauma recente, sepse, malignidade ou reação transfusional, hemorragias, trombose inexplicada, alargamento de TAP e PTT, baixa dosagem de fibrinogênio, D-dímero alto;
-
Não há alteração laboratorial patognomônica, e recomenda-se a realização de exames laboratoriais seriados para acompanhar a evolução dos parâmetros (ex.: a cada 8 horas).
| Diagnóstico de CIVD – Escore ISTH | ||
|
Exames Laboratoriais
|
Valor
|
Ponto(s) |
|
TAP
|
< 3 segundos
3-6 segundos ≥ 6 segundos |
0
1 2 |
|
D-dímero
|
Normal
Aumento discreto Aumento intenso |
0
2 3 |
|
Contagem de plaquetas
|
≥ 100.000/mm³
50.000-100.000/mm³ < 50.000/mm³ |
0
1 2 |
|
Dosagem de fibrinogênio
|
≥ 1 g/L
< 1 g/L |
0
1 |
-
Resultado:
- ≥ 5: Compatível com CIVD; repetir diariamente;
-
< 5:
Não sugestivo de CIVD; repetir a cada 1 a 2 dias.
-
Abordagem terapêutica:
- O aspecto principal é o tratamento da causa de base, a fim de eliminar o estímulo à coagulação (ex.: antibioticoterapia se sepse, quimioterapia se malignidade, indução do parto se complicações obstétricas);
- Medidas de suporte incluem hidratação vigorosa, suporte ventilatório e hemotransfusão ;
-
A administração profilática de plaquetas e/ou fatores de coagulação em indivíduos sem hemorragia e sem risco alto para hemorragia não é recomendada de rotina, exceto se trombocitopenia muito grave (< 10.000-20.000/mm³). Por outro lado, se houver sangramento ativo ou necessidade de procedimento invasivo, o uso de hemocomponentes (concentrado de plaquetas, crioprecipitado) está indicado.
Para mais informações sobre CIVD, acesse:
Coagulação intravascular disseminada
.
Disfunção Hepática
Pacientes com hepatopatia, aguda
ou crônica
, podem apresentar alteração da coagulação multifatorial (redução da produção de fatores da coagulação produzidos pelo fígado + hiperesplenismo com diminuição da quantidade de plaquetas circulantes).
Apesar disso, esses pacientes também apresentam redução dos fatores anticoagulantes, podendo apresentar-se com maior tendência pró-trombótica. Essa deficiência, no entanto, é subdiagnosticada, pois não se dosam os fatores anticoagulantes habitualmente. Assim, nesses pacientes, TAP/INR alargado não significa proteção contra eventos trombóticos ou maior risco de sangramento.
Deve ser direcionado para a causa de base. A indicação de transfusão de hemocomponentes
deve ser avaliada individualmente, tendo em vista o risco de Reações imediatas e tardias
.
-
1.
Concentrado de plaquetas (CP):
- < 10.000/mm³: Sempre considerar transfusão (exceto na púrpura trombocitopênica trombótica);
- < 20.000/mm³: Se associada a outros fatores, como febre e eventos hemorrágicos (ex.: petéquias, equimoses, sangramentos mucosos);
-
< 30.000/mm
3
:
Na leucemia promielocítica aguda
, mesmo na ausência de sangramento agudo;
-
< 50.000/mm³:
Se associada a sangramento grave (ex.: hemorragia digestiva alta
, epistaxe grave
) ou se proposta de procedimentos invasivos;
- < 80.000-100.000/mm³: Se proposta de neurocirurgia ou cirurgia oftalmológica (dependendo do procedimento).
Posologia:
1
pool
de plaquetas. Cada transfusão implica, em média, aumento de 10.000 plaquetas/mm³.
-
2.
Crioprecipitado:
- Hipofibrinogenemia (principalmente se fibrinogênio < 80 a 100 mg/dL), congênita ou adquirida (ex.: CIVD , transfusão maciça ).
Posologia:
1-1,5 unidade para cada 10 kg de peso corporal – cada unidade aumenta o fibrinogênio em 5 a 10 mg/dL, em média, sendo o alvo terapêutico > 100 a 150 mg/dL.
-
3.
Plasma fresco congelado (PFC):
- Sangramento ou risco de sangramento causado por deficiência de múltiplos fatores de coagulação (ex.: hepatopatia, CIVD );
-
Sangramento por uso de anticoagulante oral ou necessidade de reversão urgente da anticoagulação;
- Transfusão maciça com sangramento por coagulopatia dilucional;
- Púrpura trombocitopênica trombótica (como líquido de reposição na plasmaférese terapêutica);
-
Considerar se INR
> 1,5 + alto risco de sangramento, pré-procedimento invasivo ou sangramento ativo significativo.
Posologia:
10-20 mL/kg – cada unidade contém 200 a 250 mL.
Para mais informações sobre uso clínico do CP, crioprecipitado e PFC, acesse: Hemotransfusão.
-
Autoria principal:
Lívia Pessôa de Sant’Anna Coelho (Clínica Médica e Hematologia).
Galli M, Angiolillo DJ. The evaluation and management of coagulopathies in the intensive therapy units. Eur Heart J Acute Cardiovasc Care. 2023; 12(6):399-407.
Helms J, Iba T, Connors JM, et al. How to manage coagulopathies in critically ill patients. Intensive Care Med. 2023; 49(3):273-90.
Li L, Chen L, Wang H, et al. Clinical correlation between coagulation disorders and sepsis in patients with liver failure. Clin Hemorheol Microcirc. 2022; 80(3):219-231.
Iba T, Umemura Y, Wada H, et al. Roles of Coagulation Abnormalities and Microthrombosis in Sepsis: Pathophysiology, Diagnosis, and Treatment. Arch Med Res. 2021; 52(8):788-797.
Neuenfeldt FS, Weigand MA, Fischer D. Coagulopathies in intensive care medicine: balancing act between thrombosis and bleeding. J Clin Med. 2021; 10(22):5369.
Gulati D, Novak A, Stanworth SJ. Common haemostasis issues in major bleeding and critical illness. Clin Med (Lond). 2018; 18(4):320-3.
Squizzato A, Hunt BJ, Kinasewitz GT, et al. Supportive management strategies for disseminated intravascular coagulation: an international consensus. Thromb Haemost. 2016; 115(5):896-904.
Ministério da Saúde (BR). Guia para o uso de hemocomponentes. 2. ed. Brasília: MS; 2014.
Tosetto A, Castaman G, Plug I, et al. Prospective evaluation of the clinical utility of quantitative bleeding severity assessment in patients referred for hemostatic evaluation. J Thromb Haemost. 2011; 9(6):1143-8.